作者:喻俊杰、刘雪婷
近日,永利皇宫app
永利皇宫app
、生物反应器工程全国重点实验室张立新团队刘雪婷课题组,联合上海交通大学闫武鹏副教授课题组,在α-酮戊二酸依赖的单核非血红素铁酶(αKG-NHFe)催化机制研究方面取得重要进展。相关研究成果以“Structural and Mechanistic Insights into Azetidine-associated αKG-NHFe Enzyme OkaE with Multifunctional Catalysis”为题,发表于国际权威学术期刊Nature Communications。
氮杂环丁烷(azetidine)是一类在药物化学中具有重要价值的高张力含氮杂环骨架,可显著改善药物分子的构象刚性和药效学性质。然而,由于环张力大、稳定性差,其高效、可控的合成长期面临挑战。此前报道的生物合成途径中,仅有极少数酶能够构建该结构,且均依赖C–N键闭环反应。本研究首次发现,来源于真菌的αKG-NHFe酶OkaE能够通过独特的非典型C–C键偶联方式构建该环系,是目前该酶家族中唯一被证实具备此能力的成员。
研究团队通过生物化学、结构生物学与计算化学相结合的多学科交叉策略,系统解析了OkaE的多功能催化特性。研究发现,OkaE不仅能够催化氮杂环丁烷的形成,还可在同一酶体系中连续完成羟化、羧化、环氧化、环裂解等多种氧化反应,将底物转化成多种结构新颖的产物。机制研究进一步揭示,OkaE活性中心存在一组独特的甲硫氨酸–π(Met–π)相互作用网络,可精确锚定底物构象并调控其相对于金属中心的空间取向。结合晶体结构解析、定点突变实验及QM/MM计算发现,四价铁氧活性中间体FeIV=O在反应启动前发生构象旋转,是决定反应路径走向、实现多功能催化的关键步骤。
尤为引人注目的是,通过18O同位素标记实验,研究首次证实OkaE在单次催化循环中可整合第二分子氧。这种“双氧参与”模式实现在αKG-NHFe酶家族中非常罕见,为理解酶催化的复杂性提供了全新视角。该研究不仅阐明了氮杂环丁烷生物合成的分子机制,也为通过理性设计酶结构来实现天然产物的定向修饰与绿色生物制造提供了重要理论基础,对未来高效合成新型药物先导化合物具有显著的潜在应用价值。
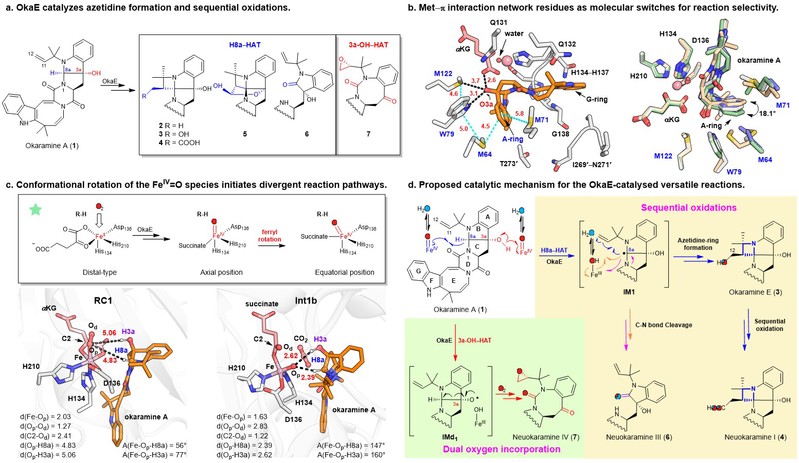
图片说明:a. OkaE催化氮杂环丁烷构建与多步连续氧化反应;b. Met–π相互作用网络中的关键残基作为调控反应选择性的分子开关;c. FeIV=O高价铁氧活性中间体构象旋转是OkaE多功能催化的关键起始步骤;d. OkaE 催化多功能反应的机制简要示意图
永利皇宫app
刘雪婷教授、上海交通大学闫武鹏副教授、永利皇宫app
朱国良博士为论文共同通讯作者;永利皇宫app
博士后王馨叶(现就职于鲁东大学)、永利皇宫app
博士生喻俊杰、上海交通大学博士生刘通海、海南大学张璇副教授为论文共同第一作者。该研究得到了上海重大专项、国家重点研发计划、国家自然科学基金、上海感染与免疫科技创新中心等项目的资助,并依托上海同步辐射光源完成相关结构数据采集。
原文链接://doi.org/10.1038/s41467-026-69519-5